Агрегатные состояния вещества
Зимой вода на поверхности озер и рек замерзает, превращаясь в лед. Подо льдом вода остается жидкой. Здесь одновременно существуют два различных агрегатных состояния воды -твердое (лед) и жидкое (вода). Существует и третье состояние воды — газообразное: невидимый водяной пар находится в окружающем нас воздухе.
Различные агрегатные состояния существуют у каждого вещества. Отличаются эти состояния друг от друга не молекулами, а тем, как эти молекулы расположены и как движутся. Особенности расположения молекул в различных агрегатных состояниях одного и того же вещества — воды — иллюстрирует рисунок 76.
При определенных условиях вещества могут переходить из одного состояния в другое. Все возможные при этом превращения отображены на рисунке 77. Буквы Т, Ж и Г обозначают соответственно твердое, жидкое и газообразное состояния вещества; стрелки указывают направление, в котором протекает тот или иной процесс.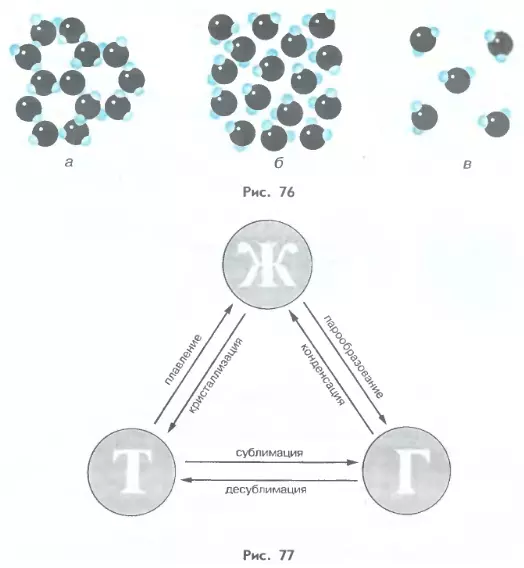
Всего различают шесть процессов, при которых происходят агрегатные превращения вещества.
Переход вещества из твердого (кристаллического) состояния в жидкое называется плавлением, обратный процесс называется кристаллизацией или отвердеванием. Пример плавления — таяние льда, обратный процесс происходит при замерзании воды.
Переход вещества из жидкого состояния в газообразное называется парообразованием, обратный процесс называется конденсацией (от латинского слова «конденсатио» — уплотнение, сгущение). Пример парообразования—испарение воды, конденсацию можно наблюдать при образовании росы.
Переход вещества из твердого состояния в газообразное (минуя жидкое) называется сублимацией (от латинского слова «сублимо» — возношу) или возгонкой, обратный процесс называется десублимацией. Например, графит можно нагреть до тысячи, двух тысяч и даже трех тысяч градусов, и тем не менее в жидкость он не превратится: он будет сублимироваться, т. е. из твердого состояния сразу переходить в газообразное. Сразу в газообразное состояние (минуя жидкое) переходит и так называемый «сухой лед» (твердый оксид углерода СО2), который можно увидеть в контейнерах для хранения и транспортировки мороженого. Все запахи, которыми обладают твердые тела (например, нафталин), также обусловлены возгонкой: вылетая из твердого тела, молекулы образуют над ним газ (или пар), который и вызывает ощущение запаха.
Примером десублимации может служить образование на окнах зимой узоров из кристалликов льда. Эти красивые узоры являются результатом десублимации водяного пара, находящегося в воздухе.
Переходы вещества из одного агрегатного состояния в другое играют важную роль не только в природе, но и в технике. Так, например, превратив воду в пар, мы можем использовать его затем в паровых турбинах на электростанциях. Расплавляя металлы на заводах, мы получаем возможность изготовить из них различные сплавы: сталь, чугун, латунь и т. д. Для понимания всех этих процессов надо знать, что происходит с веществом при изменении его агрегатного состояния и при каких условиях это изменение возможно. Об этом и пойдет речь в следующих параграфах.
1. Назовите три агрегатных состояния вещества. 2. Перечислите все возможные процессы, при которых вещество переходит из одного агрегатного состояния в другое. 3. Приведите примеры возгонки и десублимации. 4. Какие практические применения агрегатных превращений вы знаете? 5. Какой буквой (а, 6 или в) на рисунке 76 обозначено твердое состояние воды, жидкое и газообразное?
