Физика поверхностей
Для изучения физического явления не обязательно пользоваться дорогими и сложными приборами. Физика скрывается не только в блестящих приборах, но и в самой жизни, всюду вокруг нас. Надо только уметь увидеть ее. Например, сидя за чайным столом, можно наблюдать многие физические явления. Вот на тему о физике поверхностей мы и собираемся побеседовать. И пусть это будет не просто беседа. Попробуйте на собственном опыте проверить все нижеописанные явления. Прибором в данном случае может служить чашка чаю или стакан воды.
Первый взгляд на чай, налитый в чашку, подтверждает известное положение, что жидкость своей формы не имеет, а принимает форму сосуда, в который она налита. Поверхность жидкости не зависит от формы сосуда; она представляет собой гладкую, как зеркало, плоскость. Впрочем, не совсем так, форма поверхности жидкости есть форма, концентричная поверхности земного шара. Правда, чтобы подметить это, надо было бы иметь «чашку» слишком больших размеров. В обычных чашках поверхность налитой жидкости можно принимать за горизонтальную плоскость. Однако и здесь требуется поправка. Приглядитесь внимательнее, и вы заметите, что у краев поверхность жидкости приподнята и образует вогнутую форму (рис. 87). Это — следствие поверхностного натяжения, причину которого мы сейчас выясним, а пока познакомимся с еще более заметным проявлением того же свойства жидкости. Опустите в чашку чайную ложку. Вы увидите, во-первых, что поверхность жидкости искривлена в местах соприкосновения ложки с жидкостью, во-вторых, что между ложкой и стенкой чашки жидкость приподнята по сравнению с уровнем в широкой части (рис. 88). Чем ближе будет ложка к стенке чашки, тем выше поднимется уровень жидкости в узкой части. Если у вас найдется узкая стеклянная трубочка, то подъем жидкости в ней можно подметить без труда (рис. 89). В трубке диаметром 1 мм вода поднимается на 30 мм.

На высоту поднятия оказывает влияние также и температура жидкости. На 30 мм вода поднимается при 0 °C. При 80 °C она поднимется только на 25 мм.
Оказывается, с повышением температуры жидкости уменьшается поверхностное натяжение ее.
Что же такое поверхностное натяжение? На рисунке 90 в увеличенном, схематичном изображении показан вертикальный разрез жидкости. Между молекулами действуют силы взаимного притяжения, но на расстоянии не больше 5*10-8 – 10-7 см. Молекулу 1 притягивают окружающие ее со всех сторон соседние молекулы одинаково сильно. В результате эти силы притяжения уравновешиваются, или другими словами, равнодействующая всех сил молекулярного притяжения равна нулю.
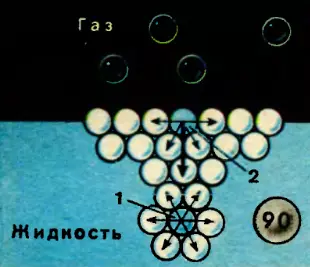
Для молекулы 2, расположенной на поверхности, равновесия молекулярных сил уже нет, и равнодействующая сил притяжения молекулы 2 ее соседними молекулами направлена вниз, в глубь жидкости. Если мы увеличиваем поверхность жидкости, а это попросту означает, что мы поднимаем из глубины на поверхность новые молекулы, то при этом мы совершаем работу против сил, направленных внутрь жидкости. Энергия, затраченная на эту работу, передается молекулам поверхностного слоя, поэтому они обладают добавочной потенциальной энергией. Это энергетическое состояние поверхностного слоя характеризуется коэффициентом поверхностного натяжения, или проще, поверхностным натяжением. Поверхностное натяжение выражается в единицах работы на единицу площади и вычисляется как работа, необходимая для увеличения площади поверхности на единицу.
Можно показать, что из определения поверхностного натяжения легко получить наименование единицы: Н/м. Действительно, Дж = Н * м, поэтому
Дж/м2 = (Н*м) / м2 = Н/м.
Следовательно, поверхностное натяжение можно выражать и в единицах силы на единицу длины.
О какой длине идет речь? Об участке длины границы, по которой жидкость соприкасается с твердым телом (например, стенками сосуда). Поверхностное натяжение показывает, с какой силой поверхностный слой стремится сократить на единицу длины свой фронт, свои границы.
«Стремление» поверхности жидкости сокращаться до возможного минимума можно наблюдать на многих явлениях. Еще Галилей задумывался над вопросом: почему капли росы, которые он видел по утрам на листьях капусты, принимают шарообразную форму? Утверждение, что жидкость не имеет своей формы, оказывается не вполне точным. Собственно форма жидкости — шар.
Из всех других геометрических форм шар обладает при данном объеме наименьшей поверхностью. Шар — наиболее емкая форма.
Небольшое количество жидкости легко образует и сохраняет шарообразную форму. Большое количество жидкости не может сохранить шарообразную форму: она изменяется под действием силы тяжести. Если устранит влияние силы тяжести, то под действием молекулярных сил жидкость принимает форму шара. Например, капли дождя в воздухе имеют форму шара. Во время падения капли все ее частицы движутся с одинаковой скоростью, а потому она не деформируется.
Условия невесомости искусственно легко воспроизводятся в следующем опыте. Жидкое масло наливают в смесь спирта и воды. Плотность этой смеси должна быть равна плотности масла. Тогда сила тяжести уравновесится выталкивающей силой и силы молекулярного притяжения образуют масляный шар, свободно парящий в смеси. Можно получить шар диаметром в несколько сантиметров. Если в масляный шар внести на проволоке небольшой диск и вращать проволоку между пальцами, то весь шар придет в движение. При этом он слегка сплющится (как сплюснуты вращающиеся вокруг своих осей планеты). Можно добиться, чтобы от шара отделилось кольцо, подобное кольцу Сатурна. Кольцо это в конце концов разорвется и распадется на несколько небольших шариков.
Впервые такой опыт был выполнен в 1849 году под руководством бельгийского ученого Плато. Сам Плато не мог любоваться столь эффективным явлением: он совершенно ослеп еще в 1843 году. Поводом, побудившим профессора к этим опытам, был такой случай. Нечаянно он налил в смесь спирта и воды небольшое количество масла, и оно приняло форму шара. Размышляя над этим фактом, Плато наметил ряд опытов, которые и были впоследствии блестяще выполнены его учениками и друзьями. Будучи слепым, Плато продолжал свои интересные исследования. В своем дневнике по поводу этого явления он записал полезное и для нас, будущие исследователи, правило: «вовремя удивляться».
Наблюдать «стремление» системы к минимуму потенциальной энергии можно и на других простых опытах, прежде всего на мыльных пузырях. Стенка мыльного пузыря, или мыльная пленка, представляет собой двойной поверхностный слой. Рамку, изготовленную из проволоки, погрузим в мыльный раствор и вынем. Она окажется затянутой довольно прочной пленкой. Бросим на нее нитяную петельку. Форма петли будет неправильная. Если же спичкой проткнуть пленку внутри петельки, то внешняя часть пленки, стремясь сократиться, растянет нитку в окружность (рис. 91). Так как окружность охватывает самую большую площадь при данном периметре, то уцелевшая часть пленки будет иметь наименьшую площадь, чем при любой другой форме петли.

Поверхностный слой воды имеет такое же свойство, как и мыльная пленка. Но поскольку образовать в нем отверстие нам не удастся, мы попробуем уменьшить поверхностное натяжение внутри петельки, брошенной на воду. Для этого надо ввести внутрь петельки ничтожное количество жидкости с меньшим, чем у воды, поверхностным натяжением, например, спирта, одеколона.
Можно проделать еще такой интересный опыт. Мелко нарезанные бумажки или какой-нибудь порошок (мука, пудра) насыпем ровным слоем на поверхность воды в стакане. Стоит коснуться поверхности воды проволочкой (или спичкой), смоченной предварительно одеколоном, и словно чудо произойдет перед вашими глазами на поверхности воды: плавающие кусочки разбегутся от проволочки. Так сократит свою поверхность слой чистой воды. Поверхность вокруг проволочки подобна круглой дырке, какую мы наблюдали в мыльной пленке.
Такое же явление можно наблюдать, если коснуться поверхности воды кусочком мыла. Последнее сильно уменьшает поверхностное натяжение воды. Вещества, которые, будучи примешаны к воде, уменьшают ее поверхностное натяжение, называются поверхностно-активными. Молекулы поверхностно-активных вещество представляют собой длинные цепочки из атомов углерода, окаймленные по всей длине атомами водорода. Концы такой цепочки имеют различные свойства (полярность). На одном из концов концентрируются кислородсодержащие группы атомов с большой химической активностью. Противоположный конец, наоборот, малоактивен, нейтрален. В результате на поверхности воды молекулы поверхностно-активных веществ, например, молекулы мыла, устанавливаются своими активными концами вниз, к воде (рис. 92), подобно поплавку рыболова, который под действием грузила устанавливается вертикально.

Приходилось ли вам мыть посуду, загрязненную жиром? Отмыть тарелку от жира чистой холодной водой трудно. Вода не смывает жир с поверхности. Если чистую воду заменить мыльной, то жир легко отмоется. Поверхностно-активное мыло оттесняет жир, занимает его место на поверхности. Мыло в отличие от жира легко растворимо в воде и легко смывается ею. Действие мыла при мытье объясняется соответствующим расположением молекул, как показано на рисунке 93.
Проделайте еще такой опыт. На поверхности воды, налитой в блюдце, опустите (осторожно) плашмя лезвие безопасной бритвы. Оно будет плавать и даже может принять на себя небольшой добавочный груз. Поверхность этой стальной пластинки покрыта незаметным для глаз слоем жира и не смачивается водой. Если к воде прибавить немного какого-нибудь поверхностно-активного вещества (мыла, спирта, керосина), опыт с лезвием не удастся, лезвие потонет.
Поверхность твердых тел может притягивать к себе и удерживать газы и пары. Это явление носит название адсорбции. В основе его лежит действие электрических сил у поверхности тела. Подробно рассматривать это действие мы сейчас не будем. Степень адсорбции, т. е. количество поглощаемого газа, зависит от природы как твердого тела, так и газа. Весьма большой способностью адсорбировать газы обладает активированный уголь (мелко раздробленный и освобожденный от смолистых примесей прокаливанием в присутствии водяного пара). Такой активированный уголь применяется в противогазах, созданных академиком Н. Д. Зелинским.
Теперь объясним явление смачивания и несмачивания жидкостями поверхности твердых тел. Рассмотрим поведение молекулы жидкости в месте соприкосновения ее с твердой стенкой. Оставляя в стороне взаимодействие этой молекулы с молекулами воздуха, мы можем сказать, что на молекулу действуют силы притяжения к молекулам жидкости и к стенке сосуда. В зависимости от того, какая из этих сил больше, будет наблюдаться смачивание или несмачивание. Найдем равнодействующую сил, действующих на нашу молекулу. В случае смачивания она будет направлена внутрь стенки. Это хорошо видно на рисунке 94 слева, где F1 — сила притяжения к молекулам стенки, а F2 — к молекулам жидкости; равнодействующая F направлена внутрь стенки. Но в таком случае молекула не может оставаться в равновесии на горизонтальной поверхности, как не может оставаться неподвижным на гладкой горизонтальной плоскости шарик, если на него нажимать пальцем с силой, направление которой составляет острый угол с горизонтальной плоскостью. Поверхность жидкости искривится так, что равнодействующая молекулярных сил будет перпендикулярна касательной к этой поверхности.

В случае несмачивания (рис. 94 справа) модуль силы F2 больше, чем силы F1; равнодействующая F направлена внутрь жидкости. Смачивающаяся жидкость образует у стенки вогнутую, несмачивающая — выпуклую форму поверхности. Только вдали от стенок поверхность жидкости горизонтальна. При достаточно близком расположении стенок друг от друга горизонтальная часть поверхности жидкости совсем исчезает и вся поверхность становится вогнутой или выпуклой, образуя так называемый мениск (луночку).
В капиллярных трубках поверхностное натяжение создает внутри жидкости, под мениском, добавочное давление. Поэтому давление под выпуклой поверхностью больше, а под вогнутой меньше, чем под плоской.
Так как давление под вогнутым мениском меньше в капилляре, чем под плоской поверхностью в сосуде, в который опущен капилляр, то смачивающая жидкость поднимается в капилляре до тех пор, пока вес столбика жидкости не уравновесит избыток под плоской поверхностью.
